由英国资助的牛津大学研究人员合作癌症研究发现了一种新机制,癌细胞可以通过这种机制适应它们在生长和对治疗产生反应时遇到的压力。这种机制涉及细胞释放小囊泡,称为外泌体。它们包含蛋白质、RNA 和其他分子的复杂混合物,可以重新编程周围的细胞。外泌体被认为由体内所有细胞释放,并在健康个体的许多过程中发挥重要作用,例如免疫和生殖。但是,在癌症中,它们会变坏并导致肿瘤生长和转移等病理变化。

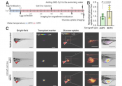
到目前为止,研究表明外泌体是在称为晚期内体的细胞隔室中产生的,它也用于通过清除细胞中受损的蛋白质和结构来保持细胞健康。通过结合果蝇和人类癌细胞的互补分析,合作团队表明外泌体也在细胞的回收系统中产生,该系统将可重复使用的蛋白质从废物处理系统中转移出来。它们被称为 Rab11a-外泌体并携带一组不同的货物,这些货物可能有助于癌症生长并在当前治疗中存活下来。
随着肿瘤变大,其中的细胞缺乏氨基酸等关键营养素,这些应激细胞会产生 Rab11a-外泌体,其中载有癌细胞产生的分子。据领导这项研究的副教授 Deborah Goberdhan 说:“这些‘坏外泌体’可以促进周围的其他细胞生长,并可能导致选择更具攻击性的细胞类型和更糟糕的结果。Rab11a 的产生-外泌体可以解释为什么有些患者对某些治疗没有反应,以及为什么其他患者经常对治疗产生耐药性。”
“越来越清楚的是,阻断生长的抗癌疗法可能需要与阻止肿瘤细胞适应疗法的药物联合使用,而减少这些外泌体的产生可能是实现这一目标的一种重要方法。”
“关键的一步将是弄清楚驱动癌症进展的坏外泌体是如何产生的,这样就可以设计治疗方法来阻止它们。这可能需要一些时间。然而,开发检测患者血液中这些外泌体的方法是一个重要的短期目标。这种方法可能会在早期发现癌症或预测患者对药物的反应,这两者都可能对癌症生存和为患者设计更个性化的治疗方案产生重大影响。”
 新传媒网
新传媒网